COVID-19
上次更新时间:2022 年 6 月。页面将每半年更新一次
It looks like you are using an older version of Internet Explorer which is not supported. We advise that you update your browser to the latest version of Microsoft Edge, or consider using other browsers such as Chrome, Firefox or Safari.
上次更新时间:2022 年 6 月。页面将每半年更新一次
Novartis 定期监测接受西尼莫德治疗的患者中 COVID-19 病例的情况。基于临床试验和上市后环境下 COVID-19 病例报告的总体可用数据,以及 MS Data Alliance GDSI 的综合数据分析1
|
截至 2022 年 3 月 25 日,累计暴露量超过 12000 患者-年,在接受西尼莫德治疗的患者中,共发现有 83 例确诊 COVID-19(SARS-CoV2 检测结果呈阳性或确诊为 COVID-19;n=79)或疑似 COVID-19 (n=4)。在 79 例确诊的 COVID-19 病例中,72 例来自 Novartis 安全性数据库。2 剩余 7 例非严重病例来自正在进行的临床试验3 |


在 262 例确诊 COVID-19 病例中,75 例是严重病例
Of the 53 confirmed COVID-19 cases, 17 were serious cases
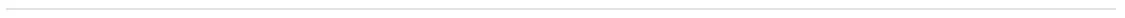
COVID-19 感染:确诊病例2,3
Novartis 定期监测临床试验或上市后接受西尼莫德治疗的患者对COVID-19疫苗的临床反应。
在CT中,320名完全接种疫苗的患者(另外45名患者接受了部分剂量的疫苗)中,有7名患者出现了突破性COVID-19感染(即第二剂疫苗接种后至少2周,或单剂量方案一次给药后至少2周)。这包括一名合并症患者,其结果为死亡,6名患者康复。
ɭ所有暴露前和暴露后的预防应根据当地指南和相应的产品信息进行。
This website is for non-promotional purposes and is intended for providing
safety information for healthcare professionals (HCPs) Only
Please confirm that you are an HCP
For HCPs: Information on this website is not country specific, and may contain information that is outside the approved indications in the country in which you are located. Please contact your local Novartis representative for the latest information specific to your country.
For non-HCPs / patients: This safety website is available for HCPs only
妊娠结局强化监测 (PRIM) 计划基于 Novartis 自发报告系统的增强药物警戒。PRIM 是一项不良事件结局强化监测计划,旨在收集妊娠即将开始前或妊娠期间暴露于西尼莫德患者的妊娠信息(目标随访清单),以及妊娠 12 个月后的婴儿结局。