AMA-VACC
中期分析结果1
Tjalf Ziemssen 等著。在西尼莫德治疗的继发性进展性多发性硬化患者中评估对SARS-CoV-2 mRNA疫苗的免疫应答(AMA-VACC 临床试验)。AAN 2022 墙报展示
SARS-COV-2 mRNA疫苗的联合免疫应答
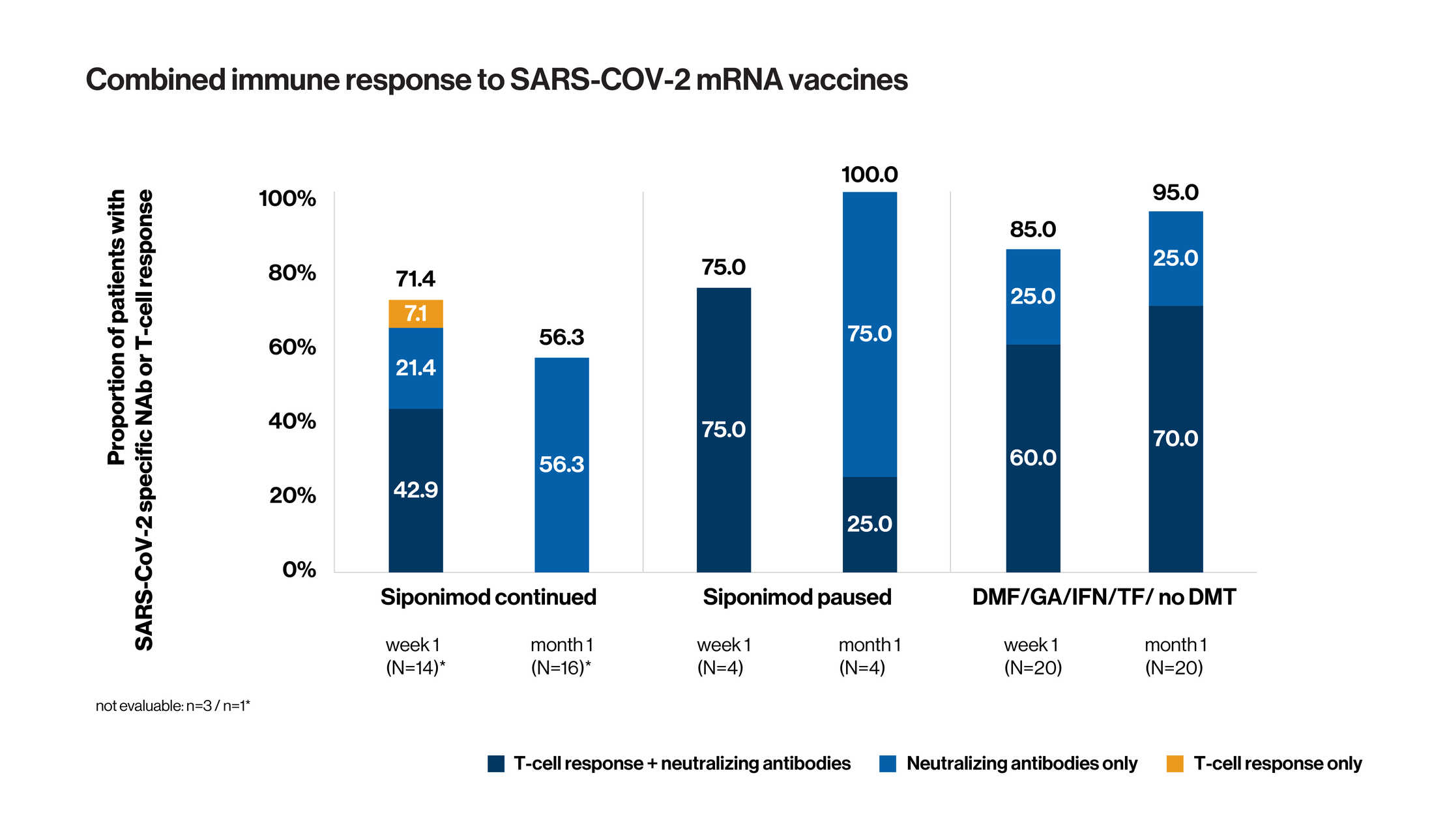
展示的数据针对具有可评价抗体和T细胞评估的患者
- AMA-VACC 临床试验在西尼莫德治疗的SPMS患者中评价了SARS-CoV-2 疫苗接种的相关数据,旨在为主治医师和患者提供MS 治疗和疫苗接种的协调指导
- 该研究在西尼莫德治疗的SPMS 患者中评估了初始和加强SARS-CoV-2 mRNA疫苗接种之后的免疫应答
- 前瞻性、开放性、三队列试验
- 中期分析包括了41名患者(17 名属于队列 1:疫苗接种期间西尼莫德治疗持续;4 名属于队列 2:因疫苗接种中断西尼莫德;还有 20 名患者属于队列 3:一线DMT/目前无治疗)
- 在 65% 的西尼莫德连续治疗患者和95% 的一线 DMT 治疗患者中,可以在某个时间点检测到中和抗体(在一周或一个月或这两个时间点)
- 观察到SARS-CoV-2 特异性 T 细胞应答的患者分别占队列 1、2和3的 50%、75% 和 60%(数据未显示)
- 总之,在完全接种后1周内,超过 70 % 的连续西尼莫德治疗的患者出现了对SARS-CoV-2 mRNA疫苗的免疫应答(即体液或细胞反应或两者)。
- 直至这项中期分析的截止日期,研究期间出现一次复发(队列 1,在末次疫苗接种 5 个月后)。
- 直至这个截止日期,没有报告COVID-19 感染,而且没有不良事件导致研究药物的永久中止
中期分析显示,服用西尼莫德的3名SPMS患者中有2名以上对SARS-CoV-2 mRNA疫苗产生免疫应答,而西尼莫德德治疗的患者可以产生体液和细胞免疫反应,评估疫苗接种效果时需要考虑这两种反应
(新)AMA-VACC 研究的中期分析