Infections
Les effets du siponimod sur le système immunitaire peuvent augmenter le risque d’infections. Un effet pharmacodynamique central du siponimod est une réduction dose-dépendante des lymphocytes périphériques en raison de la séquestration réversible des lymphocytes dans les tissus lymphoïdes.
Taux globaux d’infections dans les essais cliniques avec siponimod
Groupe contrôle1 (exposition médiane : 17 mois)
- Dans le groupe contrôle, le taux global d’infections était similaire entre les groupes siponimod et placebo.
- Le risque d’infections graves avec le siponimod était similaire à celui du placebo.
- La rhinopharyngite, l’IU, l’IVRS et la grippe étaient les infections les plus fréquentes.
- Aucun schéma particulier d’infections n’a été identifié et les événements observés étaient consistants avec les événements rapportés avec d’autres modulateurs des récepteurs de la S1P.
Groupe à long terme2 (exposition médiane : 54,6 mois)
- Au 30 octobre 2020, aucune augmentation de l’incidence globale des infections (EI apparus sous traitement et EI graves apparus du traitement) n’a été observée chez les patients traités par siponimod, ce qui était cohérent avec celui du groupe contrôle. Comme observé pendant la période contrôlée, aucun changement n’a été observé dans le type ou le schéma des infections rapportées au fil du temps.
- L’IU était l’EI grave le plus fréquemment rapporté dans le groupe siponimod.
Événements indésirables apparus sous traitement (infections)
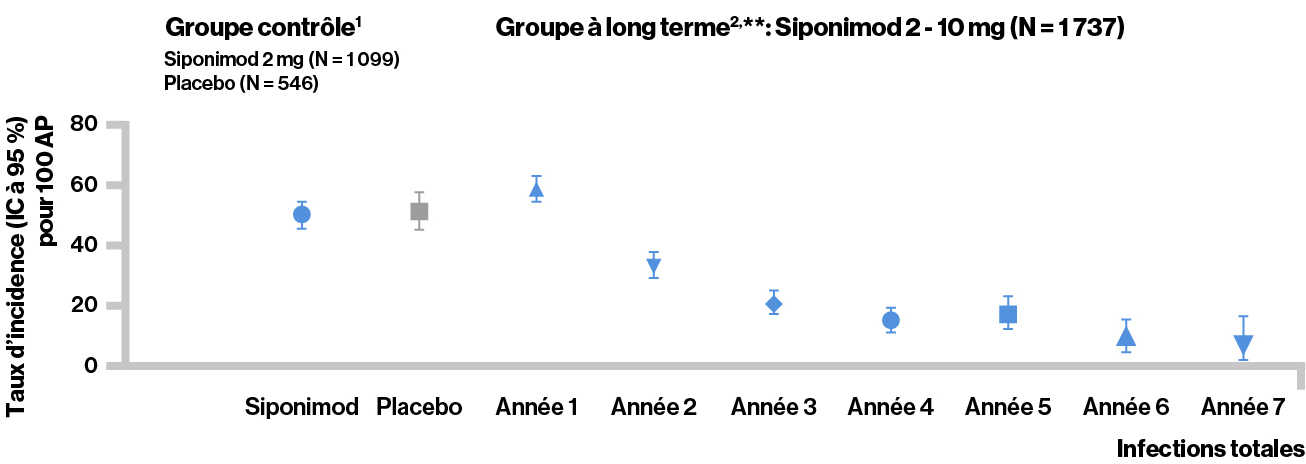
Événements indésirables graves apparus sous traitement (infections)
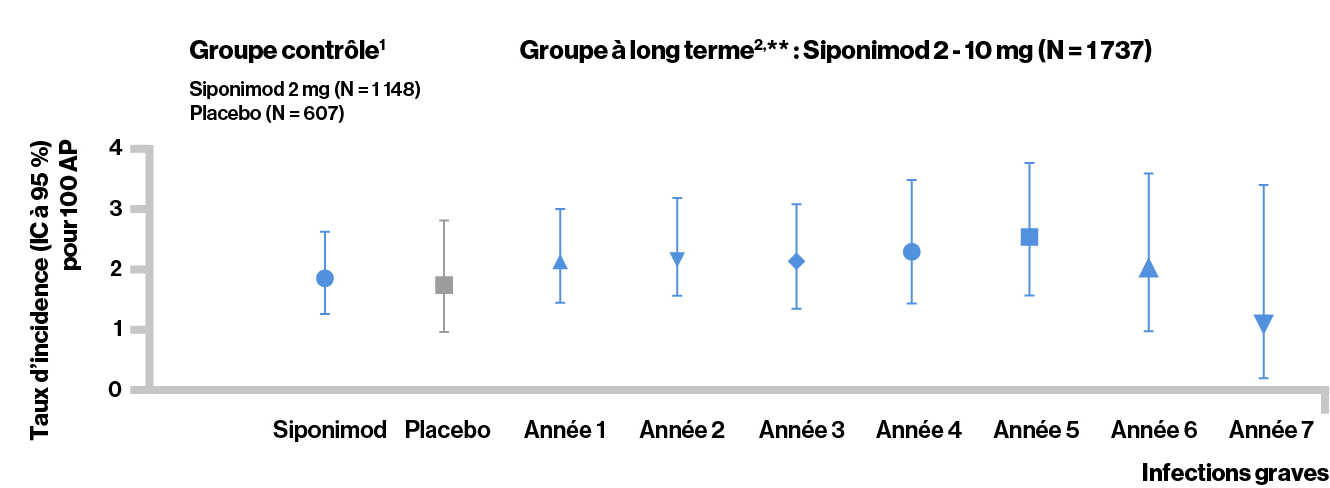
** Estimation à long terme obtenue à l’aide de la fonction d’incidence cumulée
.Le groupe contrôle 1 comprenait la partie principale en double aveugle, contrôlée par placebo, des études BOLD et EXPAND. Le groupe à long terme 2 comprenait la période de traitement par siponimod cible dans les phases principales (contrôlées et au su) et/ou d’extension des études BOLD et EXPAND.
Expérience post-AMM3
- À compter du 25 mars 2021, l’exposition estimée au siponimod chez plus de 6 000 patients atteints de SEP-R et de SEP-SP en dehors des essais cliniques correspond à 4 916 patients-années.
- Sur un total de 4 185 cas post-AMM (to be defined in the abbreviations section below) (1306 PS ; 2 879 consommateurs) présentant des EI, 478 événements étaient liés à des infections et infestations dans 407 cas (116 PS ; 291 consommateurs).
- Parmi ces événements, 59 événements dans 51 cas ont été signalés comme graves par les PS et 111 événements dans 98 cas par les consommateurs.
- Les infections graves les plus fréquemment rapportées étaient l’IU, la COVID-19 et la pneumonie.
- L’issue a été rapportée comme fatale dans 4 cas liés aux infections.
- Un patient est décédé d’une insuffisance cardiaque congestive et d’une pneumonie bronchique ; aucun détail supplémentaire n’était disponible.
- Trois patients ont présenté une issue fatale en raison de la COVID-19. L’un de ces patients était une femme de 60 ans présentant de multiples comorbidités, notamment l’obésité, le diabète et l’hypertension. Les 2 autres patients étaient âgés de plus de 50 ans et de plus de 70 ans ; aucun autre détail n’était disponible.
Taux d’infections dans la population atteinte de SEP
- Les patients atteints de SEP présentent un risque accru d’infections par rapport à une population appariée sans SEP.4,5,^
- Le taux d’incidence de toute infection était plus élevé chez les patients atteints de SEP que chez ceux sans SEP (4 805 contre 2 731 pour 10 000 personnes-années ; rapport IR [IC à 95 %], 1,76 [1,72 à 1,80]).4
^ Méthodologie de l’étude4
L’étude compare les taux d’infections chez les patients atteints de SEP après un diagnostic de SEP avec une population appariée de patients sans SEP.
The MS cohort included patients who had MS diagnosed and were treated between January 2004 and August 2017.Patients had medical history available for at least 1 year before MS diagnosis and at least La cohorte SEP comprenait des patients ayant reçu un diagnostic de SEP et traités entre janvier 2004 et août 2017. Les antécédents médicaux des patients étaient disponibles depuis au moins 1 an avant le diagnostic de SEP et avaient reçu au moins une prescription de traitement modificateur de la maladie pour la SEP. Les patients sans SEP étaient appariés aux patients atteints de SEP selon un rapport de 10:1 en fonction de l’âge, du sexe, de la région géographique et de la date d’entrée dans la cohorte. Pour chaque patient, les chercheurs ont identifié la première infection diagnostiquée de chaque type après l’entrée dans la cohorte. Les patients ont été suivis jusqu’à la perte d’éligibilité, le décès ou la fin du recueil des données. Dans l’ensemble, l’étude incluait 8 695 patients atteints de SEP et 86 934 patients appariés sans SEP. L’âge médian à l’entrée dans la cohorte était de 41 ans, et 71 % étaient des femmes. La durée médiane du suivi après l’entrée dans l’étude était d’environ 6 ans. Les patients atteints de SEP étaient plus susceptibles de présenter une infection dans l’année précédant l’entrée dans la cohorte, par rapport aux patients sans SEP (43,9 % contre 36,3 %).