EXCHANGE
中間解析結果1
Bar-Or A, et al. Safety and tolerability of conversion to siponimod in patients with relapsing multiple sclerosis: interim results of the EXCHANGE study. Poster presentation at ACTRIMS-ECTRIMS. 2020;P0233.
- EXCHANGE試験では、注射剤および経口剤のDMTからシポニモドへウォッシュアウト無しで切り替えたRMS患者、またはRMSの既往歴を有する患者を対象として、総合的な安全性および忍容性プロファイルが評価されました
-
前向き、多施設共同、非盲検、単一群試験
-
米国の42施設から113例の患者が中間解析に組み入れられ、1例は仮想群に組み入れられました
-
1件以上のAEが発現した患者(34.8%)
-
SAEおよび治験薬の投与中止に至ったAEの発現率は低かった
‒ 5例に1件以上のSAE*、6例に1件以上のAEが認められました**
-
Day-1の投与6時間後の平均心拍数は、ベースラインから顕著に低下しなかった
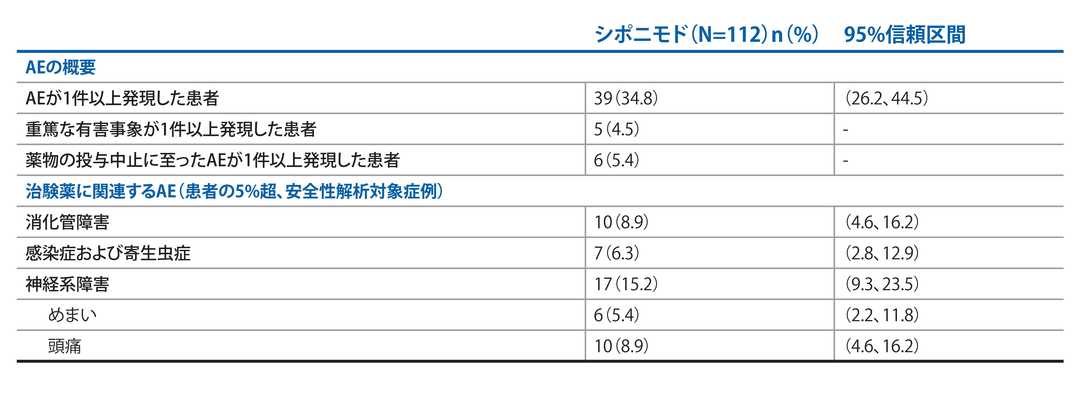
経口剤/注射剤のDMTからウォッシュアウトなしでシポニモドに切り替えた場合、安全性および忍容性プロファイルは許容範囲内であり、想定外の事象は認められなかった
(New) Latest communications of EXCHANGE in congresses
- A subgroup analysis by Race and Ethnicity of EXCHANGE: interim analysis
- A COVID-19 vaccination EXCHANGE sub-study: interim analysis
- Safety and Tolerability of Conversion to siponimod in patients with advancing forms of RMS: interim analysis
*1例の患者に複数のSAEが発現する場合がある **1例の患者に複数の投与中止に至ったAEが発現する場合がある