EXCHANGE
Ergebnisse der Zwischenanalyse1
Bar-Or A, et al. Sicherheit und Verträglichkeit der Umstellung auf Siponimod bei Patienten mit schubförmiger Multipler Sklerose: Zwischenergebnisse der EXCHANGE-Studie. Posterpräsentation auf ACTRIMS-ECTRIMS. 2020;P0233.
- EXCHANGE untersuchte das allgemeine Sicherheits- und Verträglichkeitsprofil bei Patienten mit fortschreitendem RMS oder RMS in der Vorgeschichte, die von injizierbaren und oralen DMTs auf dosistitriertes Siponimod ohne Washout umgestellt wurden.
-
Prospektive, multizentrische, offene, einarmige Studie
-
113 Patienten aus 42 Zentren in den USA in die Zwischenanalyse einbezogen; 1 Patient im virtuellen Arm
-
Patienten mit ≥ 1 UE (34,8 %)
-
SUE und UE, die zum Absetzen des Medikaments führten, waren gering.
‒ Fünf Patienten hatten ≥ 1 SUE*; sechs Patienten hatten ≥ 1 UE^
-
Keine nennenswerte Verringerung der durchschnittlichen Herzfrequenz 6 Stunden nach Tag-1-Dosis gegenüber der Baseline
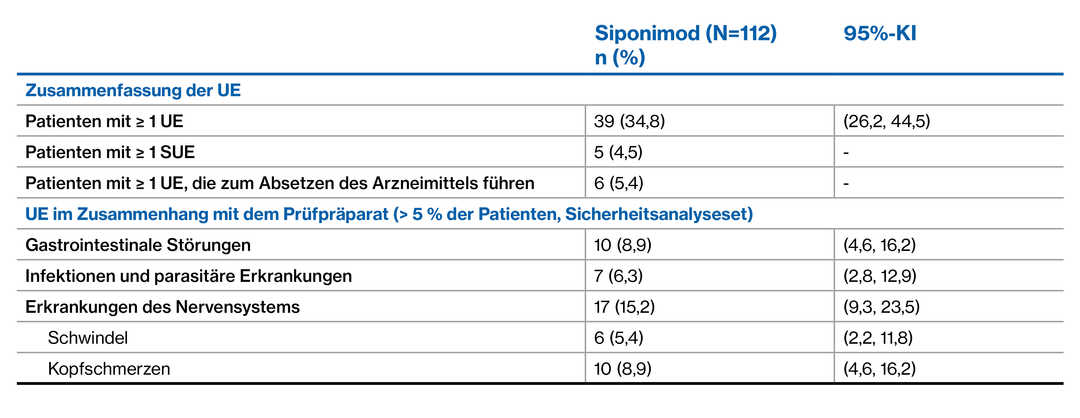
Die Umstellung von oralen/injizierbaren DMTs auf Siponimod ohne Washout wies ein akzeptables Sicherheits- und Verträglichkeitsprofil auf, ohne unbekannte Ereignisse.
(New) COVID-19 vaccination EXCHANGE sub-study
**Mehrere SUE können bei einem Patienten auftreten; ^Mehrere UE, die zum Absetzen des Medikaments führen, können bei einem Patienten auftreten